✓ Без кислорода невозможно протекание двух важнейших процессов. Значение одного из них для человеческой цивилизации подтверждает легенда о Прометее, другой − основа жизни на Земле. О каких же процессах идёт речь?
Два важнейших процесса с участием кислорода − горение и дыхание.
Проверьте свои знания
1. Назовите аллотропные модификации кислорода и сравните их свойства.
Для кислорода характерна аллотропия, т.е. образование двух простых веществ, различающихся числом атомов в молекуле: кислорода $O_$ и озона $O_$. Биологическая роль озона известка. Поэтому отметим, что озон − эффективное средство для обеззараживания питьевой воды. Кислород − газ без цвета, запаха и вкуса, немного растворимый в воде, несколько тяжелее воздуха.
2. Какое значение в природе имеет озон и где он применяется?
Озон образует тонкий слой в атмосфере Земли, защищает все живое на планете от губительного воздействия космического излучения.
В быту озон применяется для обеззараживании питьевой воды.
Настольные и интеллектуальные игры в школе: развлечение или новый подход к изучению предметов?
3. Запишите уравнения реакций получения кислорода в лаборатории. Каким образом можно: а) собрать кислород в сосуд; б) доказать наличие кислорода в сосуде?
Запишем уравнения реакций получения кислорода в лаборатории:
2$KMnO_$ = $K_$ $MnO_$ + $MnO_$ + $O_$↑
2$H_$ $O_$ = 2$H_$O + $O_$↑
2$KClO_$ = 2KCl + 3$O_$↑
а) Кислород собирается в сосуд методом вытеснения воздуха, так как он тяжелее воздуха (32>29).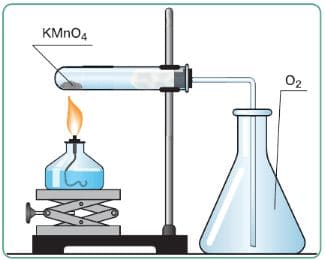
Рис. 43. Получение кислорода и собирание его методом вытеснения воздуха
б) Доказать наличие кислорода в сосуде можно с помощью тлеющей лучинки, так как кислород поддерживает горение.
Рис. 44. Получение кислорода разложением пероксида водорода и обнаружение с помощью тлеющей лучинки
4. Как кислород получают в промышленности?
В промышленности кислород получают фракционной перегонкой (или ректификацией) жидкого воздуха в специальных аппаратах, называемых ректификационными колоннами.
5. Назовите области применения кислорода.
Два важнейших процесса с участием кислорода − горение и дыхание.
Способность кислорода поддерживать горение лежит в основе применения всех видов топлива. Не менее важны процессы медленного (беспламенного) окисления различных веществ. Так, при окислении пищи в нашем организме выделяется энергия, за счёт которой организм живёт и поддерживает нужную температуру. При дыхании кислород поступает в лёгкие человека, соединяется с гемоглобином и переносится потоком крови в каждую клетку. Здесь происходит обмен молекулы кислорода в гемоглобине на молекулу углекислого газа, который, будучи токсичным продуктом жизнедеятельности, удаляется из клетки.
Растениям тоже необходим кислород. В темноте идёт процесс поглощения кислорода растениями, на свету протекает противоположный ему процесс − фотосинтез.
Именно за счёт фотосинтеза в атмосфере нашей планеты появился и поддерживается на постоянном уровне живительный кислород. Причём 80 % кислорода поставляют в атмосферу морские водоросли. Кислород совершает бесконечный круговорот на нашей планете.
Кислородный коктейль в санатории #shorts
Также кислород применяют в медицине: в оксибарокамерах, при заправке кислородных масок, для изготовления кислородных коктейлей, при выращивании микроорганизмов.
Жидкий кислород применяют в реактивных двигателях, в автогенной сварке, резке металлов.
В чистом виде кислород используют в металлургии при получении чугуна, стали, цветных металлов.
Примените свои знания
6. Запишите уравнения реакций, схемы которых:
а) $SO_$ + … → $SO_$
б) $Li_$S + … → $SO_$ + $Li_$O
в) $NaNO_$ → $NaNO_$ + …
г) $C_$ $H_$ + $O_$ → … + …
б) 2$Li_$S + 3$O_$ = 2$SO_$ + 2$Li_$O
в) 2$NaNO_$ = 2$NaNO_$ + $O_$
7. Исторически одним из самых первых способов получения кислорода была реакция разложения оксида ртути(II). Запишите уравнение этой реакции. К какому типу реакций по тепловому эффекту она относится?
2HgO = 2Hg + $O_$↑ − это эндотермическая реакция, так как происходит разложение
Используйте дополнительную информацию
8. Подготовьте сообщение по одной из тем: а) «Происхождение и изменение состава земной атмосферы»; б) «Из истории открытия кислорода»; в) «Значение кислорода в жизни».
Значение кислорода
Кислород представляет собой бесцветный газ без вкуса и запаха.
Значение этого газа для человека и живых организмов велико. Всем живым организмам кислород необходим для дыхания, так как для поддержания жизни нужно постоянное поступление кислорода, а его запасов в организме нет. Также кислород участвует в окислительных процессах, процессах горения.
Способность кислорода поддерживать горение лежит в основе применения всех видов топлива. Не менее важны процессы медленного (беспламенного) окисления различных веществ. Так, при окислении пищи в нашем организме выделяется энергия, за счёт которой организм живёт и поддерживает нужную температуру. При дыхании кислород поступает в лёгкие человека, соединяется с гемоглобином и переносится потоком крови в каждую клетку. Здесь происходит обмен молекулы кислорода в гемоглобине на молекулу углекислого газа, который, будучи токсичным продуктом жизнедеятельности, удаляется из клетки.
Растениям тоже необходим кислород. В темноте идёт процесс поглощения кислорода растениями, на свету протекает противоположный ему процесс − фотосинтез.
Именно за счёт фотосинтеза в атмосфере нашей планеты появился и поддерживается на постоянном уровне живительный кислород. Причём 80 % кислорода поставляют в атмосферу морские водоросли. Кислород совершает бесконечный круговорот на нашей планете.
Также кислород применяют в медицине: в оксибарокамерах, при заправке кислородных масок, для изготовления кислородных коктейлей, при выращивании микроорганизмов.
Жидкий кислород применяют в реактивных двигателях, в автогенной сварке, резке металлов.
В чистом виде кислород используют в металлургии при получении чугуна, стали, цветных металлов.
9. Присутствие кислорода в атмосфере Земли делает её пригодной для жизни. Однако известно и негативное влияние кислорода. Приведите примеры отрицательных явлений, связанных с наличием кислорода в воздухе. Предложите методы борьбы с этими явлениями.
Кислород жизненно необходим для человека, однако встречаются и негативные его влияния. К ним можно отнести брожение молока и образование ржавчины. Причина всему этому − участие кислорода в окислительных реакциях.
Для более длительного хранения продуктов питания их замораживают, консервируют.
Для предотвращения образования ржавчин используют лаки и специальные растворы.
Практическая работа 4
Вариант 1
1. Работу начните со сборки прибора для получения газов и проверки его герметичности. Для этого используйте подготовленную учителем пробирку−реактор с перманганатом калия. Положите в неё небольшой ватный тампон как можно ближе к отверстию, чтобы пылевидное твёрдое вещество через газоотводную трубку не попало в сосуд−приёмник для кислорода.
Собранный прибор поместите в ладонь, а конец газоотводной трубки опустите в воду. Согрейте пробирку ладонью. Появление пузырьков воздуха указывает на герметичность прибора.
2. Закрепите пробирку−реактор с веществом в лабораторном штативе, регулируя её положение так, чтобы конец газоотводной трубки доходил до дна сосуда−приёмника для кислорода.
3. Зажгите спиртовку, прогрейте пробирку−реактор, равномерно перемещая спиртовку по всей её длине. Затем установите спиртовку под ту часть пробирки, где находится перманганат калия. Нагрейте пробирку−реактор, собирая выделяющийся кислород вытеснением воздуха из сосуда. Почему кислород собирают именно так?
4. Приготовьте тлеющую лучинку. Проверьте наличие кислорода в сосуде. Для этого тлеющую лучинку опустите в сосуд. Что наблюдаете?
5. По окончании опыта погасите спиртовку и оформите отчёт по следующей форме:
Что сделал(а) Что наблюдал(а) (сделайте рисунок, если необходимо) Выводы и уравнения реакций
Используйте эту форму и при выполнении других работ.
| Собрала прибор для получения газов и проверки его герметичности. | 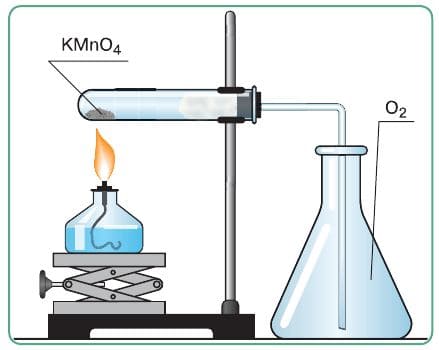 |
Прибор герметичен. |
| Закрепила пробирку−реактор с веществом в лабораторном штативе. | ||
| Зажгла спиртовку, прогрела пробирку−реактор, равномерно перемещая спиртовку по всей ее длине. Затем установила спиртовку под ту часть пробирки, где находится перманганат калия. Нагрела пробирку−реактор, собирая выделяющийся кислород вытеснением воздуха из сосуда. | Наблюдала выделение пузырьков газа − кислорода. Он собирается таким методом, так как тяжелее воздуха ( 32 > 29 ). | 2 $KMnO_$ = $K_$ $MnO_$ + $MnO_$ + $O_$ |
| Приготовила тлеющую лучинку. Проверила наличие кислорода в сосуде. | Лучинка ярко вспыхнула, так как кислород поддерживает горение. | В сосуде находится кислород. |
Вариант 2
1. Работу начните со сборки прибора для получения газов и проверки его герметичности. Для этого собранный прибор поместите в ладонь, а конец газоотводной трубки опустите в воду. Согрейте пробирку ладонью. Появление пузырьков воздуха указывает на герметичность прибора.
2. Выньте пробку с газоотводной трубкой, налейте в пробирку 3−4 мл аптечного препарата перекиси водорода, добавьте небольшое количество оксида марганца(IV) (на кончике шпателя). Быстро закройте пробирку−реактор пробкой и конец газоотводной трубки опустите в сосуд−приёмник. Что наблюдаете?
3. Соберите выделяющийся кислород вытеснением воздуха из сосуда. Почему кислород собирают именно так?
4. Приготовьте тлеющую лучинку. Проверьте наличие кислорода в сосуде. Для этого тлеющую лучинку опустите в сосуд. Что наблюдаете?
Какую роль в эксперименте играет оксид марганца(IV)? По завершении работы оформите отчёт.
| Собрала прибор для получения газов и проверки его герметичности. | Наблюдала выделение пузырьков газа.  |
Прибор герметичен. |
| Вынула пробку с газоотводной трубкой , налила в пробирку 3 − 4 мл аптечного препарата перекиси водорода, добавила небольшое количество оксида марганца (IV) ( на кончике шпателя). Быстро закрыла пробирку−реактор пробкой и конец газоотводной трубки опустила в сосуд−приёмник. | Кислород собрался в сосуде−приемнике. | Кислород собирают таким методом, так как он тяжелее воздуха ( 32 > 29 ). 2 $KMnO_$ = $K_$ $MnO_$ + $MnO_$ + $O_$ Оксид марганца (IV) является катализатором, то есть ускоряет химическую реакцию. |
| Приготовила тлеющую лучинку. Проверила наличие кислорода в сосуде. | Лучинка ярко вспыхнула, так как кислород поддерживает горение. | В сосуде находится кислород. |
- Вы здесь:
- 8 класс
- Химия
- ГДЗ ответы к учебнику химия 8 класс, Габриелян, Остроумов, Сладков
- ГДЗ ответы к рабочей тетради по химии 8 класс, Габриелян, Сладков, Остроумов
- ГДЗ ответы к рабочей тетради химия 8 класс, Габриелян, Сладков
- ГДЗ ответы к учебнику химия 8 класс, Рудзитис, Фельдман
- ГДЗ ответы к учебнику химия 8 класс, Габриелян
Источник: gdzotvet.ru
Подумайте как доказать наличие простого вещества кислорода в кислородном коктейле
Вопросы и задания
1. Напишите уравнения реакций, протекающих при сварке и резке железа с использованием ацетилено-кислородной горелки, если известно, что при горении ацетилена образуются углекислый газ и вода.
2. Горючим в некоторых ракетных двигателях служит диметилгидразин C2H8N2. Напишите уравнение реакции горения этого вещества в кислороде, если известно, что в результате образуются углекислый газ, вода и азот.
3. Как получают кислород в промышленности? Какие ещё газы можно выделить из жидкого воздуха?
4. Вентили на баллонах с кислородом категорически запрещено смазывать маслом. К каким последствиям может привести нарушение этого правила?
5. Можно ли использовать под водой ацетилено-кислородную горелку; лабораторную спиртовку? Почему?
6. Будет ли жидкий кислород, полученный из жидкого воздуха и находящийся при температуре кипения, содержать примесь аргона (Ткип = -186 °C), углекислого газа (Ткип = -79 °C), воды? С какой целью воздух перед сжижением очищают от водяного пара и углекислого газа?
7. По рисунку 42 составьте рассказ о применении кислорода. В каждом случае отметьте, на каких свойствах этого газа основано его использование.
8. Жидкий кислород немного тяжелее воды, его плотность равна 1,14 г/см 3 . Во сколько раз увеличится объём кислорода при нагревании его от -200 до 0 °C при атмосферном давлении?
Творческие задания
1. Справедливы ли утверждения: а) кислород — горючий газ; б) кислород поддерживает горение; в) жидкий кислород взрывоопасен; г) жидкий кислород имеет запах?
2. Что произойдёт с водяным паром при его попадании в жидкий кислород?
3. Кислород необходим для существования живых организмов, но в то же время он является причиной старения и разрушения клеток. О чём это свидетельствует?
4. Составьте структурные формулы двух соединений азота с водородом, в котором азот трёхвалентен.
5. Подумайте, как доказать наличие простого вещества кислорода в кислородном коктейле.
6. Атмосфера Нептуна состоит из водорода (примерно 67%), гелия (31%) и метана (2%). Назовите газ, который на Нептуне будет горючим и может быть использован для подогрева пищи на газовой плите. Запишите уравнения реакций горения. Возможно ли зажечь на Нептуне плиту, пользуясь нашими обычными спичками?
Источник: izigdz.ru
Подумайте как доказать наличие простого вещества кислорода в кислородном коктейле
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
ГДЗ к учебнику ХИМИЯ 8 КЛАСС Еремина В.В. Кузьменко Н.Е. Дроздова А.А. Лунина В.В. §20 Получение кислорода в промышленности и его применение РЕШЕБНИК ОТВЕТЫ
Красным цветом приводится решение , а фиолетовым ― объяснение.
Задание 2
Горючим в некоторых ракетных двигателях служит диметилгидразин C2H8N2. Напишите уравнение реакции горения этого вещества в кислороде, если известно, что в результате образуются углекислый газ, вода и азот.
C2H8N2 + 4O2 ⟶ 2CO2 + 4H2O + N2
Задание 3
Как получают кислород в промышленности? Из воздуха, предварительно очищенного от пыли, водяного пара и углекислого газа, который под давлением сжижают. Так как температура кипения жидкого азота (-196°С) ниже температуры кипения жидкого кислорода (-183°С), то азот испаряется, а жидкий кислород остается. Повторяя многократно процессы испарения и конденсации паров, удаётся полностью разделить жидкий воздух на азот и кислород.
Какие ещё газы можно выделить из жидкого воздуха? Азот и благородные газы.
Задание 4
Вентили на баллонах с кислородом категорически запрещено смазывать маслом. К каким последствиям может привести нарушение этого правила? Масло ― это смесь углеводородов, которые легко воспламеняются в чистом кислороде, что может привести к пожару.
Задание 5
Можно ли использовать под водой ацетилено-кислородную горелку; лабораторную спиртовку? Почему? Можно использовать ацетилено-кислородную горелку, которая содержит горючее вещество (ацетилен) и окислитель (кислород), а лабораторную спиртовку нельзя, т.к. нужен кислород для горения.
Задание 6
Будет ли жидкий кислород, полученный из жидкого воздуха и находящийся при температуре кипения, содержать примесь аргона (Tкип=-186°C), углекислого газа (Tкип=-79°C), воды? Температура кипения кислорода -183°C, поэтому кислород будет содержать примесь аргона (Tкип=-186°C). Углекислый газ и вода останутся на дне ёмкости в твёрдом состоянии.
С какой целью воздух перед сжижением очищают от водяного пара и углекислого газа? Воздух перед сжижением очищают от водяного пара и углекислого газа, потому что при сжижении воздуха они кристаллизуются, и могут перекрыть узкие трубки сжижающего аппарата.
Задание 7
По рисунку 42 составьте рассказ о применении кислорода. В каждом случае отметьте, на каких свойствах этого газа основано его использование.
Применение кислорода во время взрывных работ, в авиации и космонавтике основано на сжижении кислорода
Применение кислорода в металлургии и сварке основано на его свойствах поддерживать горение.
Применение кислорода во время подводного плавания и в медицине основано на его свойствах поддерживать дыхание.
Творческие задания
Вопрос 1
Справедливы ли утверждения:
а) кислород ― горючий газ;
Нет. Кислород не является горючим газом на Земле.
б) кислород поддерживает горение;
Да. Кислород поддерживает горение.
в) жидкий кислород взрывоопасен;
Нет. Жидкий кислород не взрывоопасен, т. к. он не является горючим газом на Земле.
г) жидкий кислород имеет запах?
Нет. Кислород имеет запах в газообразным агрегатном состоянии.
Вопрос 2
Что произойдёт с водяным паром при его попадании в жидкий кислород?
При попадании водяного пара в жидкий кислород, он замерзает (снег/лёд) .
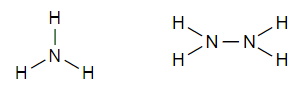
Вопрос 4
Составьте структурные формулы двух соединений азота с водородом, в котором азот трёхвалентен.
Вопрос 5
Подумайте, как доказать наличие простого вещества кислорода в кислородном коктейле. Вылить коктейль в колбу, и закрыть её пробкой с газоотводной трубкой. Нагреть колбу, и поднести тлеющую лучину к концу газоотводной трубки, при этом лучина загорится, что говорит о том, что коктейль содержит кислород.
Вопрос 6
Атмосфера Нептуна состоит из водорода (примерно 67%), гелия (31%) и метана (2%). Назовите газ, который на Нептуне будет горючим и может быть использован для подогрева пищи на газовой плите. Кислород, который будет гореть в водороде атмосферы Нептуна.
Запишите уравнения реакций горения.
2H2 + O2 = 2H2O
Возможно ли зажечь на Нептуне плиту, пользуясь нашими обычными спичками? Нельзя, так как они зажигаются в присутствии кислорода воздуха.
- Еремин Химия 8 класc 2019
- 2021-09-11
Источник: gdz.cool
